Wet MDR komt steeds dichterbij

Half maart – bij de publicatie van dit artikel – stond de invoering van de MDR op 26 mei 2020 vast. De Europese Commissie heeft de invoering van deze wet inmiddels een jaar uitgesteld in verband met de coronacrisis.
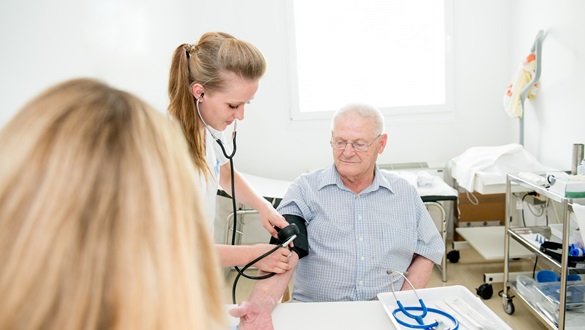
Medische hulpmiddelen worden dankzij de Medical Device Regulation (MDR) nog veiliger en gebruiksvriendelijker. Maar de nieuwe Europese richtlijn heeft ook een keerzijde. Zorgorganisaties moeten rekening houden met prijsstijgingen, minder innovaties, verschraling van het aanbod en extra werk, zo bleek uit de Kennissessie MDR voor Intrakoop-leden.
Ruim tachtig inkopers bezochten de MDR Kennissessie in Houten. De grote belangstelling is goed te verklaren. Per 26 mei 2020 is de MDR namelijk van toepassing. Dan moeten in principe (er zijn uitstelmogelijkheden) alle medische hulpmiddelen volgens de nieuwe regels gecertificeerd worden.
‘We willen de patiëntveiligheid vergroten en een goed functionerende Europese markt hebben’, verklaart Claire Hostmann, Senior beleidsmedewerker Medische technologie bij het ministerie van VWS en spreker bij deze sessie. ‘Tot nu toe waren de regels rondom medische hulpmiddelen in een richtlijn gevat. En dat leidde vaak tot interpretatieverschillen en aanvullende eisen. In de MDR formuleerden de Europese landen samen afspraken over de eisen waaraan medische hulpmiddelen moeten voldoen. Producten die hieraan voldoen zijn automatisch in alle lidstaten toegelaten.’
Patiëntveiligheid is de andere belangrijke reden voor invoering van de MDR. Vanaf 2010 waren er affaires rondom metaal-op-metaal heupimplantaten, sondevoeding en bekkenbodemmatjes. En ook het PIP-borstimplantaten schandaal uit 2012 staat nog vers in het geheugen. De nieuwe wetgeving voorziet daarom in strengere eisen en beter toezicht op de bedrijven die verantwoordelijk zijn voor de CE-markering. ‘Deze notified bodies worden allemaal opnieuw beoordeeld om te zien of ze aan de eisen voldoen.’
Distributeurs
Behalve de fabrikanten hebben ook distributeurs een hele kluif aan de MDR, zo bleek uit het verhaal van de volgende spreker, Agnes Beek, kwaliteitsmanager bij Mediq Medeco. ‘We leveren zo’n 25.000 verschillende medische hulpmiddelen die we van meer dan 400 leveranciers betrekken. De MDR heeft dus een enorme impact op ons bedrijf. Vergeleken bij de oude richtlijnen, ligt er voor distributeurs nu een veel grotere rol op bijvoorbeeld het gebied van transparantie en traceerbaarheid van producten in de keten.’
Een belangrijke taak voor distributeurs is het verifiëren van de productconformiteit. ‘Wij moeten bepalen of een product aan de eisen voldoet: Heeft het een CE-markering? Is alle informatie aanwezig om het product veilig te gebruiken? Staat er een importeur vermeld als het buiten de EU is geproduceerd? Staat er een UDI-barcode op (Unique Device Identifier, red)? Als er iets niet klopt, mogen we het product niet op de markt brengen.’ En dat is goed nieuws voor zorginstellingen. ‘Het is niet jullie taak om alles nogmaals te controleren’, sprak ze de zaal toe. ‘Jullie mogen erop vertrouwen dat wij met fabrikanten samenwerken die aan de eisen te voldoen.’
Gereedschap
De derde en laatste spreker op de kennisbijeenkomst was Addie Bouwman, expert medical devices bij Intrakoop. Hij benadrukte allereerst het belang van medische hulpmiddelen. ‘Het is het gereedschap waarmee we in de zorg het werk verrichten.’ Gereedschap waar veel geld mee gemoeid is, want volgens Bouwman geven zorgorganisaties drie keer zoveel geld uit aan medische hulpmiddelen dan aan medicijnen. ‘En bij medische hulpmiddelen denkt iedereen misschien aan MRI-scanners of andere dure apparatuur, maar het meeste geld – en ook het hoogste risico – zit in disposables.’
Bouwman vindt het goed dat de MDR er nu is. ‘Het gevolg is dat naast nog veiliger producten voor patiënten en gebruikers ook de usability geborgd is. Een veilig product heb je alleen als er ook een bekwame zorgverlener is die het op de juiste manier toepast. Er wordt daarom ook veel onderzoek gedaan naar de usability. Daardoor zal de gebruiksvriendelijkheid verder verbeteren.’ Bouwman plaatste ook de nodige kanttekeningen. ‘Al het bestaande klinisch onderzoek telt niet of nauwelijks meer mee. Dus dat moet allemaal opnieuw. Daar zijn hoge kosten mee gemoeid. De vraag is of fabrikanten die investering kunnen en willen doen. Daarnaast of ziekenhuizen bereid of in staat zijn mee te werken aan het klinisch onderzoek naar medische hulpmiddelen die ze misschien al jaren gebruiken.’ Ook wordt de traceability van de producten geoptimaliseerd en de performance in de praktijk gevolgd en vastgelegd.
Niet rendabel
Hij voorziet dat er minder producten op de markt zullen komen, omdat het voor fabrikanten niet rendabel is de hele procedure voor de MDR-certificering te doorlopen. ‘En wat dacht je van de producten die in het Verre Oosten gemaakt worden? Ik vroeg enige tijd geleden aan een aantal Chinese fabrikanten wat zij met de MDR gaan doen? Niets, was het antwoord. We richten ons gewoon op het oosten, daar wonen 2 miljard mensen.’ Fabrikanten die hun producten wel opnieuw willen laten certificeren lopen tegen het tekort aan Notified Bodies aan. Van deze zestig bedrijven die CE-certificeringen aan medische hulpmiddelen mochten toekennen, is nu slechts een handvol opnieuw geaccrediteerd. ‘Omdat het een kostbare en tijdrovende procedure is, zullen medische hulpmiddelen ook duurder worden’, aldus Bouwman, die verwacht dat het met name voor bedrijven om financiële én MDR-inhoudelijke redenen lastiger wordt met innovaties te komen en het hoofd boven water te houden.
Tips
Addie Bouwman had ook tips voor de zaal. ‘Alle producten komen op termijn met UDI-code. Vraag je systeembeheerder of het al technisch mogelijk is om deze te scannen, zodat de informatie in het systeem terechtkomt. En vraag dan meteen of klachten- en recallprocedures daaraan gekoppeld kunnen worden.’ Ook zullen zorgorganisaties deskundigheid moeten ontwikkelen op het gebied van klachtenonderzoek om goed te kunnen beoordelen waar en waarom het fout is gegaan. Verder vindt hij dat er in de opleidingen meer aandacht moet zijn voor medische hulpmiddelen. ‘Geneesmiddelen zijn onderdeel van zorgopleidingen, maar aan gereedschapsleer wordt niet of nauwelijks aandacht besteed. En net als in de farmacie, moeten ook wij gaan institutionaliseren. Ik verwacht dat elke zorgorganisatie over vijf jaar naast de apotheek ook een afdeling medische hulpmiddelen heeft. Zonder red je het niet.’
Deel dit artikel
Neem contact op
Wil je meer informatie over de MDR en de gevolgen voor je inkoop? Neem dan contact op met